Виды нтд для медицинских и фармацевтических товаров
Для медицинских и фармацевтических товаров утверждаются нормативно-технические документы.
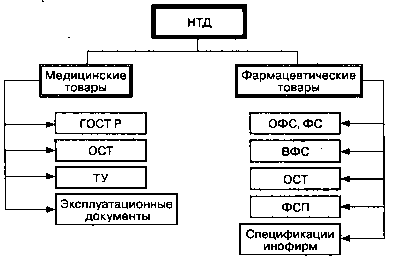
Нормативно-техническая документация на медицинские и фармацевтические товары
Нормативно-техническая документация на медицинские и фармацевтические товары
В 1973 г. был утвержден ГОСТ 19126-73 на медицинские инструменты. В нем установлены общие технические требования, которым должны соответствовать инструменты, методы контроля показателей и методы испытания инструментов, правила маркировки, упаковки, транспортировки, хранения.
В 1975 г. был утвержден ГОСТ 20790-75 «Приборы, аппараты и оборудование медицинские. Общие и технические условия». Имеются ГОСТы на перевязку, шприцы, иглы, режущие и зажимные инструменты и т.д.
Отраслевые стандарты утверждаются МЗ РФ и обязательны для предприятий и организаций медицинской промышленности.
Контроль качества готовых медицинских товаров осуществляется в соответствии с ТУ.
ТУ на медицинские изделия состоят из следующих разделов:
а) назначение изделия;
б) классификация (в случае ТУ на группу изделий);
в) основные размеры;
г) технические требования;
д) комплектность изделия;
е) правила приемки и методы испытаний;
ж) маркировка, упаковка, хранение.
Стандарт качества лекарственных средств (ЛС) — это нормативный документ, содержащий перечень нормируемых показателей и методов контроля качества ЛС, утверждаемый МЗ РФ.
Для ЛС и лекарственного растительного сырья применяются следующие виды НТД: общие фармакопейные статьи (ОФС), фармакопейные статьи (ФС), временные фармакопейные статьи (ВФС), ОСТ, фармакопейные статьи предприятий (ФСП).
ОФС — государственный стандарт качества ЛС; включает в себя перечень нормируемых показателей или методов испытания для конкретной лекарственной формы, описание физических, физико-химических, химических, биохимических, биологических, микробиологических методов анализа ЛС, требования к используемым реактивам, титрованным растворам, индикаторам.
ФС — государственный стандарт качества ЛС под международным непатентованным наименованием (МНН), содержит обязательный перечень показателей и методов контроля качества с учетом его лекарственной формы.
ФС утверждаются на ЛС, имеющие наибольшую терапевтическую ценность, широко вошедшие в медицинскую практику и имеющие высокие качественные показатели. ФС включаются в государственную фармакопею (серийное производство).
Термин «Фармакопея» происходит от греческих словpharmakon — лекарство и poieo — делаю и переводится на русский язык как руководство по приготовлению лекарств.
Государственная фармакопея (ГФ) — это сборник государственных стандартов качества ЛС, имеющий законодательный характер. В настоящее время действует ГФ XI издания (1987).
ВФС утверждаются на ЛС и лекарственное растительное сырье и на первые промышленные серии новых ЛС, рекомендованных к медицинскому применению фармакопейным комитетом и намеченных к серийному производству. Утверждаются на ограниченный срок (не более 3 лет).
ОСТ устанавливаются на дополнительные технические требования и групповые характеристики, необходимые для изготовления и поставки ЛС (термины, обозначения, правила приемки, маркировка,
упаковка, хранение, транспортирование и др.); утверждаются МЗ РФ и медицинской промышленности.
ФСП — стандарт качества на ЛС под торговым названием, содер-кащий перечень показателей и методов контроля качества ЛС, произведенного конкретным предприятием, учитывающий конкретную технологию данного предприятия и прошедший экспертизу и регистрацию в установленном порядке.
Многие страны имеютсвои национальные фармакопеи, с 1951 г. ПОЗ издает международную фармакопею. В настоящее время вышло три ее издания (1967, 1981, 1988). Международная фармакопея состоит из 5 томов: том 1 содержит общие методы анализа; 2 и 3 тома содержат спецификации для контроля качества фармакопейных препаратов (том 2 — 126 субстанций, том 3 - 157 субстанций); 4 и 5 тома содержат спецификации для контроля качества готовых лекарственных форм, вспомогательных средств и упаковочных материалов.
Для импортных ЛС к НТД относятся:
1) ГФ, ВФС;
2) зарубежные фармакопеи;
3) спецификации (статьи, нормы, сертификаты качества), разработанные иностранными фирмами.
Помимо НТД, есть еще эксплуатационные документы, которые входят в комплект изделия при выпуске их с предприятия-изготовителя. К простым изделиям, хорошо известным потребителям, прилагается этикетка (наименование изделий, обозначение изделия и его индекс, технические данные, номер стандарта или ТУ, которым соответствует изделие, сведения о приемке ОТК, сведения о количестве изделий в одной упаковке, дата выпуска).
К сложным изделиям прилагаются паспорта или формуляры.
В паспорте указывают основные параметры и характеристики изделия, далее приводятся данные, аналогичные сведениям в этикетке, гарантийные обязательства предприятий, сведения о консервации и упаковке.
Если к паспорту прилагаются журнал или листки, в которых указывается работа изделия и сведения о техническом обслуживании, то эти документы носят название формуляр. В необходимых случаях к эксплуатационным документам прилагается техническое описание (ТО), инструкция по эксплуатации (ИЭ); иногда их объединяют.